Cẩm Nang Hóa Chất
Acid Boric là gì và khi nào cần sử dụng acid boric?
Có thể đâu đó, bạn đã từng nghe qua cái tên Acid Boric. Vậy Acid Boric là chất gì và chất này có gì đặc biệt? Hãy để Hóa Chất Đại Việt giúp bạn hiểu hơn về hóa chất này nhé!
Acid Boric là gì?
Acid Boric (axit boric), loại hoá chất được tìm thấy trong các vùng có núi lửa nhất định như ở Tuscany, quần đảo Lipari và Nevada và được sử dụng rất nhiều trong các lĩnh vực như công nghiệp, y tế,.. Acid Boric là một axit yếu của nguyên tố Bo, có dạng tinh thể. Ở trạng thái thông thường không màu hoặc có màu trắng, tan trong nước.
Khi ở dạng khoáng vật, axit này có tên là sassolit. Một số tên gọi khác của Acid Boric: Orthoboric acid, Boracic acid, Optibor, Borofax.
Trong tự nhiên, Acid Boric có trong các vùng có núi lửa nhất định hoặc được trộn lẫn với hơi nước trong các khe nứt, chất này cũng tồn tại trong nước biển, thực vật và nhất là trong các loại trái cây; có mặt trong thành phần cấu tạo ở một số khoáng vật như borax, boracit,…
Tính chất của Acid Boric
Công thức hoá học
Acid Boric có công thức hoá học là: H3BO3 hoặc B(OH)3
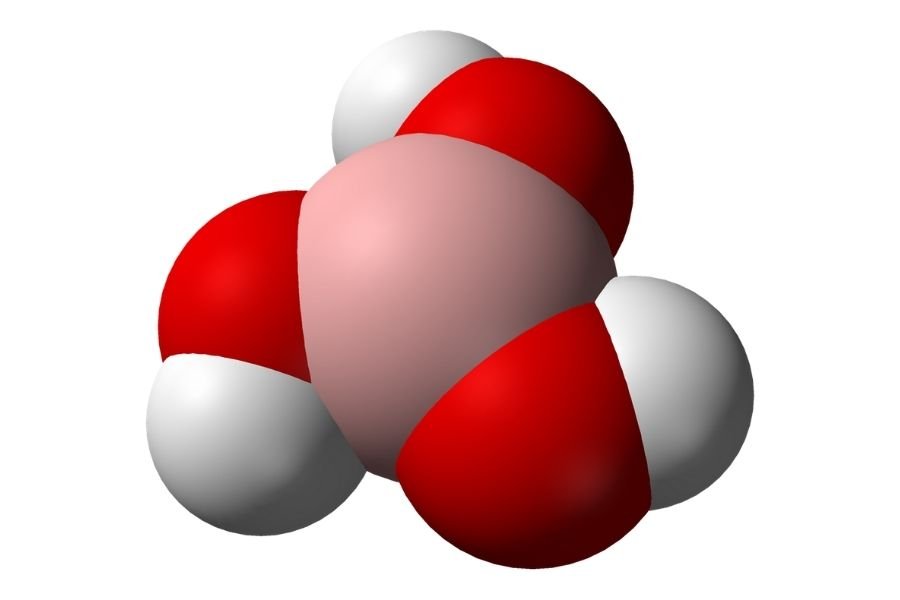
Cấu trúc tinh thể
Các phân tử B(OH)3 liên kết với nhau bằng liên kết hydro.
Khoảng cách giữa hai lớp cạnh nhau vào khoảng 318 pm.
Tính chất hóa học
Khi được nung ở nhiệt độ trên 170 độ C, H3BO3 sẽ tách nước và tạo thành axit metaboric ( HBO2 ). Phương trình phản ứng như sau:
- H3BO3 → HBO2 + H2O
Acid Boric nóng chảy ở nhiệt độ khoảng 236 độ C. Khi được nung trên nhiệt độ 300 độ C nó sẽ tiếp tục tách nước và tạo thành axit tetraboric hay axit pyroboric (H2B4O7).
- 4 HBO2 → H2B4O7 + H2O
Sau phản ứng trên, nếu tiếp tục được tách nước sẽ tạo ra boron trioxit theo phản ứng:
H2B4O7 → 2 B2O3 + H2O
H3BO3 là một axit Lewis có phản ứng với các phân tử nước, tạo thành ion tetrahydroxyborat ( được quan sát dưới quang phổ Raman ). H3BO3 không phân ly trong dung môi gốc nước.
H3BO3 cũng có vai trò quan trọng trong việc hấp thụ các sóng âm tần số thấp trong nước biển.
Sản xuất Acid Boric
Acid Boric được điều chế bằng cách cho borax phản ứng với một axit khoáng, ví dụ như axit clohidric.
Na2B4O7.10H2O + 2HCl → 4B(OH)3 [hoặc H3BO3] + 2NaCl + 5H2
H3BO3 cũng có thể được tạo ra như một sản phẩm phụ của thuỷ phân trihalides boron và diborane.
B2H6 + 6H2O → 2B(OH)3 + 6H2
BX3 + 3H2O → B(OH)3 + 3HX(X = Cl, Br, I)
Công dụng của Acid Boric
Tuy được cho vào nhóm hóa chất xử lý nước, nhưng Acid Boric – H3BO3 còn có rất nhiều công dụng nên được sử dụng trong nhiều lĩnh vực khác nhau.
Trong ngành công nghiệp dược phẩm và mỹ phẩm, H3BO3 được dùng làm thuốc khử trùng mắt, bột em bé, các chế phẩm chống lão hóa,…
Trong công nghiệp, H3BO3 được dùng trong sản xuất sành sứ, men, thuỷ tinh, da, thảm, xi măng,… và dùng trong in ấn, sơn, nhuộm, …..sản xuất phân vi lượng chứa bo, thuốc trừ sâu, vi mạch điện tử,…

Ngoài ra, Acid Boric còn được dùng làm chất bảo quản cho gỗ và sợi.
H3BO3 ức chế sự giải phóng khí dễ cháy do đốt các vật liệu xenluloza, giải phóng nước liên kết hóa học để giảm thiểu quá trình đốt cháy nhờ đó mà nó còn được dùng trong việc chữa lửa.
Trong các nhà máy hạt nhân, H3BO3 được dùng để khống chế tốc độ phân hạch của urani.
Hoá chất H3BO3 cũng được dùng làm hoá chất ban đầu để tổng hợp về chế tạo nên các hợp chất khác.
Với những giới thiệu ngắn gọn phía trên, hy vọng Hóa Chất Đại Việt đã phần nào giúp bạn hiểu rõ hơn về Acid Boric. Nếu bạn có nhu cầu sử dụng hóa chất này với chất lượng tốt cùng giá cả phải chăng, hãy liên hệ ngay với chúng tôi nhé!


